Synthetische Cannabinoide in Europa
Introduction
Analyse: Synthetische Cannabinoide in Europa

Bei synthetischen Cannabinoid-Rezeptor-Agonisten (im Allgemeinen als „synthetische Cannabinoide“ bezeichnet) handelt es sich um eine Gruppe von Stoffen, welche die Wirkungen von (–)-trans-Δ9-Tetrahydrocannabinol (THC) imitieren. THC ist die Substanz, die vor allem für die wesentlichen psychoaktiven Wirkungen von Cannabis verantwortlich ist. Wie auch THC binden sich synthetische Cannabinoide an die Cannabinoid-Rezeptoren im Körper. Dies ist der Grund dafür, dass diese Substanzen verwendet werden, um vielzählige „Legal High“-Produkte herzustellen, die als legale Ersatzmittel für Cannabis verkauft werden. Es ist die größte Gruppe neuer psychoaktiver Substanzen, die von der Europäischen Beobachtungsstelle für Drogen und Drogensucht (EMCDDA) überwacht werden.
„Legal High“-Produkte, die synthetische Cannabinoide enthalten, wurden seit Mitte der 2000er als „Räuchermischungen auf Kräuterbasis“ vertrieben. Diese Produkte enthalten kein Cannabis, haben jedoch ähnliche Wirkungen, wenn sie geraucht werden. Diese werden mit innovativen Vermarktungsstrategien angepriesen und sind einfach und ohne Probleme im Internet sowie in einigen Ländern in konventionellen Geschäften (die vielfach als „Headshops“ oder „Smartshops“ bezeichnet werden) erhältlich.
Die Anzahl der synthetischen Cannabinoide, ihre chemische Vielfalt und die Geschwindigkeit ihres Auftauchens am Markt machen die Erkennung und Überwachung von und die Reaktion auf diese Gruppe von Verbindungen besonders schwierig. Lieferanten zielen allein darauf ab, die Wirkungen von THC zu imitieren. Im Grunde macht dies alle synthetischen Cannabinoide frei verfügbar. Wenn ein synthetisches Cannabinoid gesetzlich kontrolliert wird oder kurz davor steht, verfügen die Hersteller über einen oder mehrere verkaufsbereite Ersatzstoffe.
Es ist nur wenig über die Wirkungsweise dieser Substanzen und ihre toxischen Auswirkungen auf den Menschen bekannt. Jedoch hat ihr Konsum zu vielen schweren Vergiftungen und sogar Todesfällen geführt — in einigen Fällen kam es zum Ausbruch von Massenvergiftungen. Es ist möglich, dass einige dieser Substanzen neben ihren hohen Wirksamkeitsgraden auch lange Halbwertzeiten haben, was potenziell zu einer verlängerten psychoaktiven Wirkung führen kann. Darüber hinaus scheint es, dass mindestens einige dieser Substanzen über die Wirkungen auf die Cannabinoid-Rezeptoren hinaus auch Wirkungen auf die Körperfunktionen haben.
In dieser Analyse sollen der aktuelle Kenntnisstand betreffend diese Substanzen und ihre Wirkungen sowie Trends im Zusammenhang mit ihrer Herstellung, ihrer Verfügbarkeit und ihrem Konsum zusammengefasst werden.
Die Entstehung synthetischer Cannabinoide
Trotz Gerüchten im Internet seit Mitte der 2000er, die von „Räuchermischungen auf Kräuterbasis“ sprachen, die als „Legal High“-Produkte verkauft werden und starke cannabisähnliche Wirkungen haben, wurde das synthetische Cannabinoid JWH-018 erst im Jahr 2008 von Kriminaltechnikern in Deutschland und Österreich in einem Produkt, das unter dem Handelsnamen „Spice“ vertrieben wurde, nachgewiesen (1). Im Anschluss daran wurden unterschiedliche Cannabinoide in Räuchermischungen oder in sogenanntem Räucherwerk zur Raumluftaromatisierung entdeckt. Typische Produkte waren Spice Gold, Spice Silver und Yucatan Fire, denen später noch viele andere folgten. Viele der Cannabinoide, die in diesen Produkten nachgewiesen wurden, wurden zuerst von Wissenschaftlern entwickelt, die untersuchten, wie Cannabinoide auf den Körper wirken und ob sie als Arzneimittel zur Behandlung einer Reihe von Krankheiten und deren Symptomen, wie etwa bei neurodegenerativen Erkrankungen, Drogenabhängigkeit, Schmerzerkrankungen und Krebs, wirksam sein könnten. Es hat sich bisher jedoch als schwierig erwiesen, die gewünschten therapeutischen Eigenschaften von den unerwünschten psychoaktiven Wirkungen zu trennen.
Synthetische Cannabinoide sind die größte Gruppe von Substanzen, die derzeit durch das EU-Frühwarnsystem für neue psychoaktive Substanzen überwacht werden. Im Jahr 2008 wurde 1, 2009 wurden 9, 2010 wurden 11, 2011 wurden 23, 2012 wurden 30, 2013 wurden 29, 2014 wurden 30, 2015 wurden 25 und 2016 wurden 11 neue synthetische Cannabinoide gemeldet. Im Dezember 2016 waren der EMCDDA insgesamt 169 synthetische Cannabinoide bekannt (2).
Synthetische Cannabinoide spielen eine wichtige Rolle auf dem rasch wachsenden Markt für „Legal High“-Produkte. „Legal High“ ist ein Sammelbegriff für nicht regulierte (neue) psychoaktive Substanzen, die in der Regel die Wirkung kontrollierter Drogen imitieren und auf dem freien Markt verkauft werden. In diesem Bereich liegen nur wenige Daten über den Konsum vor. Risiken und Schädigungen sind weitgehend unbekannt, hohe Wirksamkeitsgrade geben jedoch Anlass zur Sorge. Im Falle der Räuchermischungen, die synthetische Cannabinoide enthalten, können zum Beispiel innerhalb einer Charge und zwischen verschiedenen Chargen des Produkts sowohl die Substanzen als auch die vorhandene Menge stark variieren.
Herstellung synthetischer Cannabinoidprodukte
Die meisten synthetischen Cannabinoide, die in „Legal High“-Produkten verwendet werden, werden von Chemieunternehmen mit Sitz in China hergestellt. Sie werden in Form von pulverförmigem Schüttgut in Express-Sendungen und mit Kurierunternehmen nach Europa geliefert; größere Mengen können als Luft- oder Seefracht versendet werden. Es werden häufig Sendungen mit mehreren Kilogramm von den Behörden in Europa abgefangen. Obwohl die Reinheit dieses pulverförmigen Schüttguts selten bestimmt wird, berichtete eine Studie aus Südkorea von Reinheitsgraden zwischen 75 % und 90 % für Proben pulverförmigen Schüttguts (3). Im Jahr 2015 fanden in Europa über 24 000 Beschlagnahmen synthetischer Cannabinoide statt (24 210); dies entspricht einem Gesamtgewicht von über 2,3 Tonnen (2334 kg), wovon über 400 kg (444,245 kg) auf pulverförmiges Schüttgut entfielen. Dies entspricht gegenüber dem Jahr 2014 einem Anstieg von fast 7000 Beschlagnahmen und über 1,6 Tonnen (die überwiegend aus pflanzlichem Material bestanden).
Die Produkte für den Verkauf an die Konsumenten werden erst in Europa gemischt. Damiana (Turnera diffusa) und Lippenblütler wie Melissen, Minzen und Thymiane (4) dienen häufig als Kräuterbasis für die Räuchermischungen. Die synthetischen Cannabinoide werden mit Pflanzenmaterial vermischt oder darauf gesprüht. Dabei wird typischerweise in industriellem Maßstab auf Lösungsmittel wie Aceton oder Methanol zur Lösung des Pulvers zurückgegriffen. Danach werden Geräte wie Betonmischmaschinen verwendet, um die Inhaltsstoffe zu vermischen. Danach wird die Mischung getrocknet und verpackt. Sie werden dann im Internet bei „Legal High“-Händlern oder in konventionellen Head-Shops verkauft.
Aufgrund des hohen Wirksamkeitsgrads einiger synthetischer Cannabinoide kann die pro Verpackungseinheit benötigte Pulvermenge in der Größenordnung einiger Dutzend Milligramm liegen. Das heißt, dass aus jedem Kilogramm Pulver somit Tausende Packungen von „Legal High“-Produkten hergestellt werden können. Die Aushebung von Verarbeitungs- und Verpackungseinrichtungen sowie die Sicherstellung großer Mengen synthetischer Cannabinoide in den Niederlanden und Belgien lassen Rückschlüsse auf eine Beteiligung der organisierten Kriminalität am Vertrieb zu. Es liegen auch Hinweise auf einen schwunghaften Internet-Einzelhandel in Europa vor, wo Zoll- und Polizeibehörden regelmäßig kleinere Produktmengen sicherstellen.
Die systematische Überwachung von Onlineshops, die „Legal High“-Produkte vertreiben, bietet einen Einblick in das Verkaufsangebot an Räuchermischungen, von denen wahrscheinlich viele synthetische Cannabinoide enthalten. Eine solche Überwachung in Kombination mit Testkäufen aus dem Produktangebot schafft zudem die Möglichkeit, die Veränderung der in einem Produkt enthaltenen Substanzen im Zeitverlauf zu beobachten und bei der Früherkennung von Cannabinoiden, die neu am Markt sind, zu helfen.
Prävalenz
Die Informationen zum Ausmaß, in dem synthetische Cannabinoidprodukte konsumiert werden, sind begrenzt. Die Kenntnis der Situation verbessert sich jedoch zunehmend, da immer mehr Länder Fragen über den Konsum neuer Drogen in ihre Erhebungen in der Allgemeinbevölkerung aufnehmen. Aus den gegenwärtig vorliegenden Informationen lässt sich ableiten, dass die Prävalenz ihres Konsums in der Allgemeinbevölkerung in Europa gering ist. Es wurde eine Reihe von Umfragen zur Analyse der Prävalenz des Konsums von „Spice“-ähnlichen Produkten durchgeführt, doch deren Erfassungsgrad und Repräsentativität sind noch beschränkt.
Hinsichtlich der Prävalenz des Konsums synthetischer Cannabinoide bestehen zwischen dem europäischen und dem amerikanischen Drogenmarkt erhebliche Unterschiede. Die aktuellsten Prävalenzdaten aus den USA stammen aus der 2014 unter Schülern durchgeführten Studie „Monitoring the Future“ und lassen mit Ergebnissen von 5,8 % im Jahr 2014, 7,9 % im Jahr 2013 und 11,3 % im Jahr 2012 auf eine abnehmende 12-Monats-Prävalenz des Konsums synthetischer Cannabinoide bei den 17- und 18-Jährigen schließen (29). Laut derselben Erhebung war im Jahr 2011 „synthetisches Marihuana“ die am zweithäufigsten konsumierte Droge nach Cannabis, mit einer 12-Monats-Prävalenz von 11,4 %.
Mehrere Studien aus europäischen Ländern enthalten Daten über den Konsum synthetischer Cannabinoide. Diese sind aufgrund der unterschiedlichen verwendeten Methoden, Stichprobengrundlagen und Begrifflichkeiten jedoch nicht vergleichbar. Insgesamt deuten die einzelnen Studien jedoch auf sehr niedrige Prävalenzraten hin. Das Vereinigte Königreich (England und Wales) fragte in zwei aufeinanderfolgenden Haushaltserhebungen nach dem Konsum von „Spice“. Dabei ergab sich eine Lebenszeitprävalenz von 0,2 % in den Jahren 2010/2011 bzw. 0,1 % in den Jahren 2011/2012 bei Erwachsenen (16 bis 64 Jahre) (6,7). Im British Crime Survey for England and Wales (britische Straftatenerhebung für England und Wales), der 2014/2015 abdeckte, hatten insgesamt 0,9 % der Erwachsenen (16 bis 59 Jahre) im vorherigen Jahr neue psychoaktive Substanzen konsumiert, wobei 61 % eine Räuchermischung auf Kräuterbasis konsumiert hatten (8). Aufgrund der geringen Prävalenzrate wurde die Frage in den Folgejahren nicht mehr in den Fragebogen aufgenommen.
In Spanien wurden im Jahr 2014 im Rahmen einer nationalen Erhebung zum Drogenkonsum unter Schülern im Alter von 14–18 Jahren mit einer Stichprobengröße von 37 486 geringe Raten beim Konsum von „Spice“-Produkten festgestellt, mit einer Lebenszeitprävalenz von 0,8 % im Jahr 2014, was einen Rückgang gegenüber 1,4 % im Jahr 2012 und 1,1 % im Jahr 2010 bedeutet (9,32). Bei einer Erhebung in der Allgemeinbevölkerung, die im Jahr 2013 ebenfalls in Spanien durchgeführt wurde, gaben 0,5 % der 23 136 Teilnehmer (im Alter von 15 bis 64 Jahren) an, mindestens einmal im Leben Spice konsumiert zu haben (10).
Eine in Frankreich im Jahr 2014 durchgeführte Erhebung unter Erwachsenen (18–64) mit einer Frage zum Konsum „synthetischer Cannabinoide“ ergab eine Lebenszeitprävalenz von 1,7 %. Erstkonsumenten dieser neuen synthetischen Produkte sind zumeist Männer (2,3 % Männer gegenüber 1,2 % Frauen) der jüngsten Generation (unter 35 Jahre): Von den 18- bis 34-Jährigen haben 4,0 % synthetische Cannabinoide ausprobiert, während es bei den 35- bis 64-Jährigen nur 0,6 % sind (11). In einer weiteren Umfrage in Frankreich gaben Jugendliche im Alter von 17 Jahren an, dass 1,7 % von ihnen schon ein synthetisches Cannabinoid konsumiert haben (12).
In der Erhebung des Schwedischen Rats für Informationen über Alkohol und andere Drogen (CAN) aus dem Jahr 2015 wurden Schüler zu ihrem Konsum neuer psychoaktiver Substanzen befragt. Dabei wurde in der 9. und 11. Klasse mit 1,6 % bzw. 3,2 % im Hinblick auf Teilnehmer, die angaben, zu einem beliebigen Zeitpunkt konsumiert zu haben, ein Rückgang gegenüber anderen Jahren festgestellt. Synthetische Cannabinoide waren laut den Angaben der Teilnehmer in der 9. Klasse und des zweiten Jahrs der oberen Sekundarstufe die am häufigsten konsumierte neue psychoaktive Substanz (37).
In Frankfurt am Main wurde der Konsum von Räuchermischungen und „Spice“ bei Schülern im Alter von 15 bis 18 Jahren untersucht. Dabei ergab sich unter den Befragten eine Lebenszeitprävalenz von 7 % im Jahr 2009, 9 % im Jahr 2010 und je 7 % in den Jahren 2011 und 2012 (13,14,15). Im Jahr 2013 ging die Lebenszeitprävalenz beim Konsum von Räuchermischungen auf 5 % zurück, stieg jedoch im Jahr 2014 auf 6 % an und blieb im Jahr 2015 bei 6 %; dies liegt jedoch weiterhin unter den Werten von 2009–2012 (16,17, 33). Bei Schülern, die „Spice“ konsumiert hatten, handelte es sich großteils um erfahrene Cannabiskonsumenten.
Im Übrigen wurde bei Studien unter bestimmten Personengruppen (Partygänger, Internetnutzer usw.) mit nicht probabilistischen Stichproben generell ein höherer Konsum synthetischer Cannabinoide als in der Allgemeinbevölkerung festgestellt. Im Rahmen der Global Drug Survey 2012 ergab sich beispielsweise bei der 12-Monats-Prävalenz ein Wert von 3,3 % für alle Teilnehmer aus dem Vereinigten Königreich (nicht repräsentativ für die Allgemeinbevölkerung). Demgegenüber stand ein Wert von 5,0 % bei regelmäßigen Partygängern im Vereinigten Königreich (18).
Im Vereinigten Königreich gibt der Konsum synthetischer Cannabinoide unter Häftlingen besonderen Anlass zu Bedenken. Im Rahmen einer 2016 in den Gefängnissen des Vereinigten Königreichs durchgeführten Erhebung wurde festgestellt, dass 33 % der 625 Insassen angaben, innerhalb des vorherigen Monats „Spice“ konsumiert zu haben (verglichen mit 14 %, die angaben, im vorherigen Monat Cannabis konsumiert zu haben). Die Prävalenz des Konsums von „Spice“ innerhalb des vorherigen Monats schwankte von Gefängnis zu Gefängnis zwischen 15 % und 71 %. Jene Teilnehmer, die angaben, innerhalb des vorherigen Monats „Spice“ konsumiert zu haben, wurden nach der wöchentlichen Konsumhäufigkeit gefragt; die Ergebnisse zeigten, dass 31 % „Spice“ einmal oder zweimal wöchentlich konsumiert hatten; 8 % hatten einmal wöchentlich konsumiert, 15 % zwei- bis dreimal wöchentlich und 46 % fast täglich (30). Im Rahmen einer Studie, die im Jahr 2015 vom HM Inspectorate of Prisons durchgeführt wurde, wurden 1376 Häftlinge in acht Gefängnissen befragt; dabei wurde festgestellt, dass 10 % in ihrem jeweiligen Gefängnis „Spice“ konsumierten (31).
Schädliche Auswirkungen synthetischer Cannabinoide
Die gesundheitsschädigenden Auswirkungen synthetischer Cannabinoide sind zum einen auf die intrinsischen Eigenschaften der Substanzen (was der Körper mit den Substanzen macht) und zum anderen auf die Vorgehensweise bei der Herstellung der Produkte zurückzuführen. Im Zusammenhang mit dem Konsum wurde über zahlreiche nicht tödliche Vergiftungen und eine geringere Anzahl an Todesfällen berichtet (19,20). Da einige dieser Verbindungen eine enorme Wirksamkeit aufweisen, besteht ein hohes Potenzial für toxische Effekte. Diese Risiken kommen noch zum Herstellungsprozess hinzu, der zu einer ungleichen Verteilung der Substanzen im Pflanzenmaterial führen kann. Dies kann bei einigen Produkten mit „Hot Pockets“, bei denen das Cannabinoid hoch konzentriert ist, zu Dosen führen, die höher als beabsichtigt sind und das Risiko schwerer gesundheitsschädigender Auswirkungen erhöhen (21,22). Es ist auch möglich, dass einige der gesundheitsschädigenden Auswirkungen durch andere Mechanismen als die Interaktion mit den Cannabinoid-Rezeptoren, wie z. B. durch die Störung anderer Körperfunktionen, verursacht werden (23).
Eine aktuelle systematische Überprüfung der gesundheitsschädigenden Auswirkungen im Zusammenhang mit synthetischen Cannabinoiden kam zu dem Ergebnis, dass Agitiertheit (Aufregung), Übelkeit und ein ungewöhnlich schneller Herzschlag häufig berichtete Vergiftungssymptome waren (17), während schwere gesundheitsschädigende Auswirkungen — wie etwa Schlaganfall, Krämpfe, Herzinfarkt, Abbau von Muskelgewebe, Nierenschaden, Psychose und schweres oder lang anhaltendes Erbrechen — sowie damit im Zusammenhang stehende Todesfälle weniger häufig waren 17). Es wurde über Symptome, die auf eine Abhängigkeit hinweisen, sowie über Entzugserscheinungen berichtet (22). Insgesamt ist es schwierig zu schätzen, wie häufig diese gesundheitsschädigenden Auswirkungen sind, u. a. da die Anzahl der Menschen mit Exposition gegenüber diesen Drogen unbekannt ist (17).
Eine der auffälligsten Eigenschaften synthetischer Cannabinoide ist ihre Fähigkeit, Ausbrüche von Massenvergiftungen zu verursachen. Manchmal sind Hunderte von Menschen über einen kurzen Zeitraum betroffen, was in den vergangenen Jahren in den Vereinigten Staaten und Russland ein großes Problem gewesen ist. Im Jahr 2014 wurden in Russland mehr als 600 Vergiftungen, einschließlich 15 Todesfälle, über einen Zeitraum von zwei Wochen auf das Cannabinoid MDMB-FUBINACA zurückgeführt (23). Anfang 2016 wurde diese Substanz auf dem europäischen Markt identifiziert, was die EMCDDA zu einem Gesundheitsalarm in ihrem Frühwarn-Netzwerk veranlasste. Im Jahr 2015 kam es zu einem weiteren großen Ausbruch in den Vereinigten Staaten, der scheinbar teilweise auf eine Substanz zurückzuführen war, die als ADB-FUBINACA bezeichnet wird (24,25). Während diese Arten von Ausbrüchen in Europa selten zu sein scheinen, wurden 2015 innerhalb von weniger als einer Woche mehr als 200 Notfälle in Krankenhäusern gemeldet, nachdem Menschen in Polen ein Produkt mit der Bezeichnung „Mocarz“ geraucht hatten.
Im Juli 2016 war MDMB-CHMICA der erste synthetische Cannabinoid-Rezeptor-Agonist, für den von der EMCDDA eine Risikobewertung durchgeführt wurde (35); für diesen Stoff wurden kürzlich Kontrollmaßnahmen und strafrechtliche Sanktionen in ganz Europa eingeführt (36). MDMB-CHMICA wird als wirkstarker und vollständiger Agonist am CB1-Rezeptor eingestuft und ist außerdem nachweislich ein Agonist am CB2-Rezeptor. Zum Zeitpunkt der Bewertung waren der EMCDDA 25 akute Intoxikationen und 28 Todesfälle gemeldet worden, die mit MDMB-CHMICA in Verbindung gebracht wurden. In 12 der Fälle wurde MDMB-CHMICA entweder als Todesursache oder als wahrscheinlicher Faktor genannt, der zum Tod beigetragen hat. In drei Fällen wurde MDMB-CHMICA als einzige Substanz nachgewiesen. MDMB-CHMICA ist auf dem Drogenmarkt der Europäischen Union seit spätestens August 2014 erhältlich, und zum Zeitpunkt der Risikobewertung war die Substanz in 23 Mitgliedstaaten sowie in der Türkei und in Norwegen nachgewiesen worden. Die der EMCDDA und Europol gemeldeten Informationen legten nahe, dass über 120 kg MDMB-CHMICA beschlagnahmt worden waren, wobei ca. 67 kg als pflanzliches Material und ca. 46 kg in Pulverform vorlagen. Die größte einzelne Beschlagnahme von Schüttgut, die der EMCDDA gemeldet wurde und bei der es sich um 40 kg hochreines, MDMB-CHMICA enthaltendes Pulver handelte, stammte aus China (34).
Die EMCDDA-Überwachung schwerer gesundheitsschädigender Auswirkungen und die aktuelle Kenntnis der pharmakologischen und toxikologischen Wirkungen einiger synthetischer Cannabinoide zeigen, dass diese Verbindungen schwere schädliche Auswirkungen auf die menschliche Gesundheit haben können. Allerdings sind die Mechanismen, wie es dazu kommt, bisher weitgehend ungeklärt.
Aktuelle Entwicklungen
Seit dem Auftauchen des Phänomens der synthetischen Cannabinoide am Markt waren diese Substanzen hauptsächlich in Produkten enthalten, die unter der Bezeichnung „Räuchermischungen auf Kräuterbasis“ vertrieben werden. In jüngster Zeit wurde jedoch aus mehreren Ländern berichtet, dass diese Substanzen auch in Produkten nachgewiesen wurden, die den Anschein erwecken, es handle sich um Cannabisharz, und zwar entweder in Form von „Legal High“-Produkten wie „Afghan Incense“ oder auf dem illegalen Markt, wo sie als Cannabisharz ausgegeben werden. Diese Entwicklung ist vermutlich eine Reaktion auf die Beliebtheit von Cannabisharz in vielen Ländern. Synthetische Cannabinoide wurden auch in Gemischen gefunden, die andere neue psychoaktive Substanzen enthalten, wie Stimulanzien, Halluzinogene und Sedativa/Hypnotika. Dies könnte sowohl beabsichtigt als auch unbeabsichtigt sein. In einigen wenigen Fällen wurden synthetische Cannabinoide auch in Tabletten oder Kapseln nachgewiesen, bei denen es sich anscheinend um Ecstasy handelt. In Ungarn und den Vereinigten Staaten hat dies zu Anhäufungen akuter Vergiftungen geführt (26). Eine weitere neue Entwicklung ist der Nachweis synthetischer Cannabinoide in den Liquids, die in den Kartuschen für E-Zigaretten enthalten sind. Dies ist sehr wahrscheinlich auf die in letzter Zeit wachsende Beliebtheit des „Dampfens“ bei jungen Leuten zurückzuführen.
Die EMCDDA beobachtet die Entwicklungen in Bezug auf synthetische Cannabinoide seit deren Identifizierung auf dem europäischen Markt 2008 genau. Dabei erwies sich die Weiterentwicklung und Anpassung dieser Chemikalienfamilie als faszinierend. Klar ist, dass die innovativen chemischen Substitutionsmuster dieses Phänomens in Zukunft eine engmaschige Überwachung neuer Entwicklungen in diesem Bereich, einschließlich der durch synthetische Cannabinoide verursachten Schädigungen, erfordern.
Footnotes
- (1) EMCDDA (2009), Understanding the ‚Spice‘ phenomenon, EMCDDA Thematic Paper, Amt für Veröffentlichungen der Europäischen Union, Luxemburg.
- (2) Zum Zweck der Überwachung im Rahmen des EU-Frühwarnsystems wird der Begriff „synthetische Cannabinoide“ hier für Folgendes verwendet: die große Anzahl an synthetischen Cannabinoid-Rezeptor-Agonisten (wie etwa JWH-018, bei dem es sich um einen CB1- und CB2-Rezeptor-Agonisten handelt), die auf dem europäischen Drogenmarkt identifiziert wurden; eine wesentlich kleinere Anzahl an allosterischen Modulatoren (wie etwa Org 27569), welche die Struktur der Cannabinoid-Rezeptoren ändern, was zu einer veränderten Aktivität führt, wenn ein Ligand an die Rezeptoren bindet; und Substanzen, die als Inhibitoren von Fettsäureamid-Hydrolase (FAAH), dem für den Abbau des Endocannabinoids Anandamid verantwortlichen Enzym, wirken (wie etwa URB597). Diese Drogenperspektive behandelt ausschließlich synthetische Cannabinoid-Rezeptor-Agonisten.
- (3) Choi, H., Heo, S., Choe, S., et al. (2013), ‘Simultaneous analysis of synthetic cannabinoids in the materials seized during drug trafficking using GC-MS’, Analytical and Bioanalytical Chemistry, 405(12), S. 3937–3944.
- (4) Ogata, J., Uchiyama, N., Kikura-Hanajiri, R. und Goda, Y. (2013), ‘DNA sequence analyses of blended herbal products including synthetic cannabinoids as designer drugs’, Forensic Science International, 227(1–3), S. 33–41.
- (5) National Institute on Drug Abuse (2014), ‘Monitoring the Future Survey 2014, overview of findings’, NIDA, Bethesda, MD, USA.
- (6) Smith, K. und Flatley, J. (eds) (2011), Drug misuse declared: Findings from the 2010/11 British Crime Survey, England and Wales, Home Office, London.
- (7) Office for National Statistics (2012), Drug misuse declared: Findings from the 2011/12 Crime Survey for England and Wales, Home Office, London.
- (8) Home Office (2015), ‘Tables for drug misuse: Findings from the 2014 to 2015 CSEW’, Home Office, London.
- (9) Spanish Observatory on Drugs (2012), Survey on drug use among Secondary School Students in Spain 2012 (ESTUDES).
- (10) Spanish Observatory on Drugs (2013), Survey on Alcohol and Drugs in Spain (EDADES)
- (11) Beck, F., Richard, J.-B., Guignard, R., Le Nezet, O. und Spilka, S. (2015), ‘Levels of drugs use in France in 2014’, Tendances 99.
- (12) Spilka, S., Le Nézet, O., Ngantcha, M. und Beck, F. (2015), ‘Drug use in 17-year-olds: Analysis of the ESCAPAD survey’, Tendances 100.
- (13) Werse, B., Müller, O., Schell, C. und Morgenstern, C. (2011), Jahresbericht MoSyD: Drogentrends in Frankfurt am Main 2010, Centre for Drug Research, Frankfurt am Main.
- (14) Werse, B., Bernard, C., Schell-Mack, C. und Morgenstern, C. (2012), MoSyD Jahresbericht 2011: Drogentrends in Frankfurt am Main, Centre for Drug Research, Frankfurt am Main.
- (15) Bernard, C., Werse, B. und Schell-Mack, C. (2013), MoSyD Jahresbericht 2012: Drogentrends in Frankfurt am Main, Centre for Drug Research, Frankfurt am Main.
- (16) Werse, B., Morgenstern, C. und Sarvari, L. (2014), MoSyD Jahresbericht 2013: Drogentrends in Frankfurt am Main, Centre for Drug Research, Frankfurt am Main.
- (17) Werse, B., Kamphausen, G., Egger, D., Sarvari, L. und Müller, D. (2015), MoSyD Jahresbericht 2014: Drogentrends in Frankfurt am Main, Centre for Drug Research, Frankfurt am Main.
- (18) Guardian/Mixmag Survey (2012), abgerufen am 13. März 2013.
- (19) Tait, R. J., Caldicott, D., Mountain, D., Hill, S. L., Lenton, S. (2016), ‘A systematic review of adverse events arising from the use of synthetic cannabinoids and their associated treatment’, Clinical Toxicology (Philadelphia) 54(1), S. 1–13.
- (20) American Association of Poison Control Centers (n.d.), ‘Synthetic cannabinoids’, AAPCC, Alexandria, VA.
- (21) Lindigkeit, R. 1., Boehme, A., Eiserloh, I., et al. (2009), ‘Spice: A never ending story?’, Forensic Science International, 191(1–3), S. 58–63.
- (22) Uchiyama, N., Kikura-Hanajiri, R., Ogata, J. und Goda, Y. (2010), ‘Chemical analysis of synthetic cannabinoids as designer drugs in herbal products’, Forensic Science International, 198(1–3), S. 31–38.
- (23) Fisar, Z. (2010), ‘Inhibition of monoamine oxidase activity by cannabinoids’, Naunyn Schmiedeberg’s Archives of Pharmacology, 381(6), S. 563–572.
- (24) Macfarlane, V. und Christie, G. (2015), ‘Synthetic cannabinoid withdrawal: A new demand on detoxification services’, Drug and Alcohol Review 34(2), S. 147–153.
- (25) Shevyrin, V., Melkozerov, V., Nevero, A., et al. (2016), ‘Identification and analytical characteristics of synthetic cannabinoids with an indazole-3-carboxamide structure bearing a N-1-methoxycarbonylalkyl group’, Analytical and Bioanalytical Chemistry 407(21), S. 6301–6315.
- (26) Kasper, A. M., Ridpath, A. D., Arnold, J. K., et al. (2015), ‘Severe illness associated with reported use of synthetic cannabinoids: Mississippi, April 2015’, Morbidity and Mortality Weekly Report 64(39), S. 1121–1122.
- (27) Drug Enforcement Administration (2015), ‘Proposed rule schedules of controlled substances: Temporary placement of the synthetic cannabinoid MAB-CHMINACA into Schedule I’, Federal Register 80(179), S. 55565–55568.
- (28) Brenneman, R., Papsun, D. M., Logan, B. K. und Neavyn, M. J. (2016), ‘Death-like slumber: Toxic outbreak of AB-FUBINACA’, Journal of Medical Toxicology, 12(1), S. 39.
- (29) Johnston, L. D., O'Malley, P. M., Miech, R. A., Bachman, J. G., & Schulenberg, J. E. (2016). Monitoring the Future national survey results on drug use, 1975–2015: Overview, key findings on adolescent drug use. Ann Arbor: Institute for Social Research, The University of Michigan, S. 98. Abrufbar unter: http://www.monitoringthefuture.org/pubs/monographs/mtf-overview2015.pdf.
- (30) User Voice (2016), Spice: the bird killer. What prisoners think about the use of spice and other legal highs in prison. Abrufbar unter: http://www.uservoice.org/news/user-voice-news-blog/2016/05/nhs-report-by-user-voice-hears-directly-from-inmates-the-true-horrors-of-nps-use-in-prisons/.
- (31) HM Inspectorate of Prisons (2015). Changing patterns of substance misuse in adult prisons and service responses. A thematic review by HM Inspectorate of Prisons, December 2015. Abrufbar unter: https://www.justiceinspectorates.gov.uk/hmiprisons/wp-content/uploads/sites/4/2015/12/Substance-misuse-web-2015.pdf.
- (32) Spanish Obervatory on Drugs (2016) ESTUDES 2014/15. USID Encuesta sobre uso de drogas en enseñanzas secundarias en España. Abrufbar unter: http://www.pnsd.msssi.gob.es/profesionales/sistemasInformacion/sistemaInformacion/pdf/2016_Informe_ESTUDES.pdf.
- (33) Werse, B., Egger, D., Sarvari, L., Kamphausen, G., und Müller, D. (2016), MoSyD Jahresbericht 2015: Drogentrends in Frankfurt am Main, Centre for Drug Research, Frankfurt am Main.
- (34) Gemeinsamer Bericht der EMCDDA und von Europol zu Methyl 2-[[1-(cyclohecylmethyl)indol-3-carbonyl]amino]-3,3-dimethylbutanoat (MDMB-CHMICA). EMCDDA–Europol , Lissabon, Juli 2016. Abrufbar unter: http://emcdda.europa.eu/publications/joint-reports/mdmb-chmica.
- (35) EMCDDA (2017). Bericht über die Risikobewertung von Methyl 2-[[1-(cyclohecylmethyl)-1H-indol-3-carbonyl]amino]-3,3-dimethylbutanoat im Rahmen des Beschlusses des Rates über neue psychoaktive Substanzen. Abrufbar unter: [Link einfügen, sobald verfügbar].
- (36) Durchführungsbeschluss des Rates (EU) 2017/369 vom 27. Februar 2017 über Kontrollmaßnahmen für Methyl 2-[[1-(cyclohecylmethyl)-1H-indol-3-carbonyl]amino]-3,3-dimethylbutanoat (MDMB-CHMICA). Amtsblatt der Europäischen Union L 56/210 vom 3.3.2017, abrufbar unter: http://eur-lex.europa.eu/legal-content/EN/TXT/HTML/?uri=CELEX:32017D0369&qid=1489767473947&from=EN.
- (37) Public Health Agency of Sweden (2016), Drugs workbook, Stockholm, unveröffentlicht.
Interaktiv: Chemische Zusammenhänge leicht gemacht
Interaktive Grafik wird geladen … bitte warten!
Zum besseren Verständnis der Chemie der synthetischen Cannabinoide wird hier ein Modell verwendet, das helfen soll, den chemischen Aufbau dieser Verbindungen zu erklären. Synthetische Cannabinoide unterscheiden sich chemisch. Allen gemeinsam ist jedoch ihre Fähigkeit, an die Cannabinoid-Rezeptoren anzudocken. Allerdings lässt sich der Aufbau eines Großteils der synthetischen Cannabinoide in vier Hauptelemente unterteilen: Rumpf und Substituenten, Bindeglied, Ring und Substituenten sowie Rest Bei der Auswahl der richtigen Molekülkomponenten ergibt sich ein synthetisches Cannabinoid.
Hinweis: Ein zweiter Klick auf ein Molekül kehrt die Auswahl um.
| Cannabinoid | Core | Core Substituent | Link | Ring system | Ring substituent | Tail |
|---|---|---|---|---|---|---|
| Apinaca | indazole | : | carboxamide | adamantyl | : | pentyl |
| 5F-APINACA (5F-AKB48) | indazole | : | carboxamide | adamantyl | : | 5-fluoropentyl |
| AM-2201 indazolecarboxamide analogue | indazole | : | carboxamide | naphthyl | : | 5-fluoropentyl |
| A-834,735 | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | tetrahydropyran-4-yl methyl |
| JWH-015 | indole | : | methanone | naphthyl | : | propyl |
| AM-679 | indole | : | methanone | phenyl | 2-iodo | pentyl |
| Apica | indole | : | carboxamide | adamantyl | : | pentyl |
| JWH-018 | indole | : | methanone | naphthyl | : | pentyl |
| JWH-007 | indole | 2-methyl (core-substituent) | methanone | naphthyl | : | pentyl |
| JWH-018 adamantoyl derivative | indole | : | methanone | adamantyl | : | pentyl |
| AM-6527 | indole | : | carboxamide | naphthyl | : | pentyl |
| AM-6527 5F derivative | indole | : | carboxamide | naphthyl | : | 5-fluoropentyl |
| PB-22 | indole | : | carboxylate | quinolinyl | : | pentyl |
| JWH-081 | indole | : | methanone | naphthyl | 4-methoxy | pentyl |
| JWH-122 | indole | : | methanone | naphthyl | 4-methyl | pentyl |
| JWH-182 | indole | : | methanone | naphthyl | 4-propyl | pentyl |
| JWH-203 | indole | : | ethanone | phenyl | 2-chloro | pentyl |
| JWH-210 | indole | : | methanone | naphthyl | 4-ethyl | pentyl |
| JWH-250 | indole | : | ethanone | phenyl | 2-methoxy | pentyl |
| JWH-251 | indole | : | ethanone | phenyl | 2-methyl (ring-substituent) | pentyl |
| JWH-387 | indole | : | methanone | naphthyl | 4-bromo | pentyl |
| JWH-398 | indole | : | methanone | naphthyl | 2-chloro | pentyl |
| JWH-412 | indole | : | methanone | naphthyl | 4-fluoro | pentyl |
| RCS-4 | indole | : | methanone | phenyl | 4-methoxy | pentyl |
| RCS-4 ortho isomer | indole | : | methanone | phenyl | 2-methoxy | pentyl |
| UR-144 | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | pentyl |
| JWH-022 | indole | : | methanone | naphthyl | : | pent-4-enyl |
| JWH-122 pentenyl 2-methylindole derivative | indole | 2-methyl (core-substituent) | methanone | naphthyl | 4-methyl | pent-4-enyl |
| JWH-122 pentenyl derivative | indole | : | methanone | naphthyl | 4-methyl | pent-4-enyl |
| UR -144 (-2H) | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | pent-4-enyl |
| AM-1220 Azepane Isomer | indole | : | methanone | naphthyl | : | methylazepan-3-yl |
| AB-005 azepane isomer | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | methylazepan-3-yl |
| 3-(p-Methoxybenzoyl)-N-methylindole | indole | : | methanone | phenyl | 4-methoxy | methyl |
| JWH-019 | indole | : | methanone | naphthyl | : | hexyl |
| UR-144 heptyl derivative | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | heptyl |
| BB-22 | indole | : | carboxylate | quinolinyl | : | cyclohexylmethyl |
| JWH-073 | indole | : | methanone | naphthyl | : | butyl |
| JWH-073 methyl derivative | indole | : | methanone | naphthyl | 4-methyl | butyl |
| RCS-4(C4) | indole | : | methanone | phenyl | 4-methoxy | butyl |
| 5FUR-144 | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | 5-fluoropentyl |
| AM-2201 | indole | : | methanone | naphthyl | : | 5-fluoropentyl |
| AM-694 | indole | : | methanone | phenyl | 2-iodo | 5-fluoropentyl |
| AM-694 ethyl substituted for iodine | indole | : | methanone | phenyl | 2-ethyl | 5-fluoropentyl |
| AM-694 methyl substituted for iodine | indole | : | methanone | phenyl | 2-methyl (ring-substituent) | 5-fluoropentyl |
| MAM-2201 | indole | : | methanone | naphthyl | 4-methyl | 5-fluoropentyl |
| STS-135 | indole | : | carboxamide | adamantyl | : | 5-fluoropentyl |
| EAM-2201 | indole | : | methanone | naphthyl | 4-ethyl | 5-fluoropentyl |
| 5F-PB22 | indole | : | carboxylate | quinolinyl | : | 5-fluoropentyl |
| AM-694 chloro derivative | indole | : | methanone | phenyl | 2-iodo | 5-chloropentyl |
| JWH 018 N-(5-chloropentyl) derivative | indole | : | methanone | naphthyl | : | 5-chloropentyl |
| MAM-2201 chloropentyl derivative | indole | : | methanone | naphthyl | 4-methyl | 5-chloropentyl |
| UR-144 N-(5-chloropentyl) derivative | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | 5-chloropentyl |
| JWH 018 N-(5-bromopentyl) derivative | indole | : | methanone | naphthyl | : | 5-bromopentyl |
| AM-2232 | indole | : | methanone | naphthyl | : | 4-cyanobutyl |
| A-796,260 | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | 2-morpholin-4-yl ethyl |
| JWH-200 | indole | : | methanone | naphthyl | : | 2-morpholin-4-yl ethyl |
| WIN 48,098 / Pravadoline | indole | 2-methyl (core-substituent) | methanone | phenyl | 4-methoxy | 2-morpholin-4-yl ethyl |
| AB-005 | indole | : | methanone | cyclopropyl | 2,2,3,3-tetramethyl | methylpiperidin-2-yl methyl |
| AM-1220 | indole | : | methanone | naphthyl | : | methylpiperidin-2-yl methyl |
| AM-1248 | indole | : | methanone | adamantyl | : | methylpiperidin-2-yl methyl |
| AM-1248 azepane isomer | indole | : | methanone | adamantyl | : | methylazepan-3-yl |
| AM-2233 | indole | : | methanone | phenyl | 2-iodo | methylpiperidin-2-yl methyl |
| JWH-250 1-(2-methylene-N-methyl-piperidyl) derivative | indole | : | ethanone | phenyl | 2-methoxy | methylpiperidin-2-yl methyl |
| CRA-13 | naphthalene | : | methanone | naphthyl | : | pentoxy |
| JWH-307 | pyrrole | 5-(2-fluoro)phenyl | methanone | naphthyl | : | pentyl |
| JWH-370 | pyrrole | 5-(2-methyl)phenyl | methanone | naphthyl | : | pentyl |
| JWH-368 | pyrrole | 5-(3-fluoro)phenyl | methanone | naphthyl | : | pentyl |
| JWH-307 bromine analogue | pyrrole | 5-(2-bromo)phenyl | methanone | naphthyl | : | pentyl |
| JWH-030 | pyrrole | : | methanone | naphthyl | : | pentyl |
| JWH-145 | pyrrole | 5-phenyl | methanone | naphthyl | : | pentyl |
| AB-PINACA | indazole | : | carboxamide | carbamoyl | isopropyl | pentyl |
| ADB-FUBINACA | indazole | : | carboxamide | carbamoyl | tert-butyl | fluorobenzyl |
| ADB-PINACA | indazole | : | carboxamide | carbamoyl | tert-butyl | pentyl |
| AB-CHMINACA | indazole | : | carboxamide | carbamoyl | isopropyl | cyclohexylmethyl |
| ADB-CHMINACA | indazole | : | carboxamide | carbamoyl | tert-butyl | cyclohexylmethyl |
| MDMB-CHMICA | indole | : | carboxamide | methoxycarbonyl | tert-butyl | cyclohexylmethyl |
| 5F-MDMB-PINACA | indazole | : | carboxamide | methoxycarbonyl | tert-butyl | 5-fluoropentyl |
| MDMB-FUBINACA | indazole | : | carboxamide | methyl-3,3-dimethylbutanoate | : | fluorobenzyl |
| CUMYL-4CN-BINACA | indazole | : | carboxamide | CUMYL | : | 4-cyanobutyl |
| CUMYL-4CN-BINACA | indazole | : | carboxamide | CUMYL | : | 4-cyanobutyl |
| MO-CHMINACA | indazole | : | carboxylate | methoxycarbonyl | tert-butyl | cyclohexylmethyl |
| Apinaca | cannabinoid |
/sites/default/files/Apinaca.png |
371 | 517 | apinaca |
| 5F-APINACA (5F-AKB48) | cannabinoid | /sites/default/files/AKB-48Fv2.png | 391 | 528 | akb48f |
| AM-2201 indazolecarboxamide analogue | cannabinoid | /sites/default/files/AM-2201%2520indazolecarboxamide.png | 425 | 528 | am2201inda |
| A-834,735 | cannabinoid | /sites/default/files/A-834_735.png | 357 | 396 | a834735 |
| JWH-015 | cannabinoid | /sites/default/files/JWH-015.png | 356 | 455 | jwh015 |
| AM-679 | cannabinoid | /sites/default/files/AM-679.png | 356 | 425 | am679 |
| Apica | cannabinoid | /sites/default/files/apicaV2.png | 371 | 517 | apica |
| JWH-018 | cannabinoid | /sites/default/files/jwh-018v2.png | 356 | 517 | jwh018 |
| JWH-007 | cannabinoid | /sites/default/files/JWH-007.png | 356 | 517 | jwh007 |
| JWH-018 adamantoyl derivative | cannabinoid | /sites/default/files/JWH-018-adamantoyl-derivativeV2.png | 356 | 467 | jwh018adade |
| AM-6527 | cannabinoid | /sites/default/files/AM-6527.png | 425 | 517 | am6527 |
| PB-22 | cannabinoid | /sites/default/files/PB-22.png | 425 | 517 | pb22 |
| JWH-081 | cannabinoid | /sites/default/files/JWH-081.png | 445 | 517 | jwh081 |
| JWH-122 | cannabinoid | /sites/default/files/JWH-122.png | 409 | 517 | jwh122 |
| JWH-182 | cannabinoid | /sites/default/files/JWH-182.png | 498 | 517 | jwh182 |
| JWH-203 | cannabinoid | /sites/default/files/JWH-203.png | 356 | 517 | jwh203 |
| JWH-210 | cannabinoid | /sites/default/files/JWH-210.png | 445 | 517 | jwh210 |
| JWH-250 | cannabinoid | /sites/default/files/JWH-250.png | 409 | 517 | jwh250 |
| JWH-251 | cannabinoid | /sites/default/files/JWH-251.png | 356 | 517 | jwh251 |
| JWH-387 | cannabinoid | /sites/default/files/JWH-387.png | 409 | 517 | jwh387 |
| JWH-398 | cannabinoid | /sites/default/files/JWH-398.png | 356 | 517 | jwh398 |
| JWH-412 | cannabinoid | /sites/default/files/JWH-412.png | 409 | 517 | jwh412 |
| RCS-4 | cannabinoid | /sites/default/files/RCS-4.png | 445 | 425 | rcs4 |
| RCS-4 ortho isomer | cannabinoid | /sites/default/files/RCS-4%2520ortho%2520isomer.png | 356 | 425 | rcs4oriso |
| UR-144 | cannabinoid | /sites/default/files/UR-144.png | 350 | 447 | ur144 |
| JWH-022 | cannabinoid | /sites/default/files/JWH-022.png | 356 | 517 | jwh022 |
| JWH-122 pentenyl 2-methylindole derivative | cannabinoid | /sites/default/files/JWH-122%2520pentenyl%25202-methylindole.png | 409 | 517 | jwh122p2md |
| JWH-122 pentenyl derivative | cannabinoid | /sites/default/files/JWH-122%2520pentenyl.png | 409 | 517 | jwh122pd |
| UR -144 (-2H) | cannabinoid | /sites/default/files/UR-144%2520(-2H).png | 350 | 447 | ur1442h |
| AM-1220 Azepane Isomer | cannabinoid | /sites/default/files/AM-1220%2520azepane%2520isomer.png | 356 | 513 | am1220azis |
| AB-005 azepane isomer | cannabinoid | /sites/default/files/AB-005%2520azepane%2520isomer.png | 350 | 443 | ab005azeiso |
| 3-(p-Methoxybenzoyl)-N-methylindole | cannabinoid | /sites/default/files/3-%28p-methoxybenzoyl%29-N-methylindole.png | 445 | 301 | 3pmnm |
| JWH-019 | cannabinoid | /sites/default/files/JWH-019.png | 391 | 528 | jwh019 |
| UR-144 heptyl derivative | cannabinoid | /sites/default/files/UR-144%2520heptyl.png | 408 | 509 | ur144hep |
| BB-22 | cannabinoid | /sites/default/files/BB-22.png | 425 | 466 | bb22 |
| JWH-073 | cannabinoid | /sites/default/files/JWH-073.png | 356 | 466 | jwh073 |
| JWH-073 methyl derivative | cannabinoid | /sites/default/files/JWH-073%2520methyl.png | 409 | 466 | jwh073met |
| RCS-4(C4) | cannabinoid | /sites/default/files/RCS-4%2520(C4)(1).png | 445 | 374 | rcs4c4 |
| 5FUR-144 | cannabinoid | /sites/default/files/5FUR-144.png | 391 | 458 | 5fur144 |
| AM-2201 | cannabinoid | /sites/default/files/AM-2201.png | 391 | 528 | am2201 |
| AM-694 | cannabinoid | /sites/default/files/AM-694.png | 391 | 436 | am694 |
| AM-694 ethyl substituted for iodine | cannabinoid | /sites/default/files/AM-694%2520ethyl%2520for%2520iodine.png | 391 | 436 | am694ethio |
| AM-694 methyl substituted for iodine | cannabinoid | /sites/default/files/AM-694%2520methyl%2520for%2520iodine.png | 391 | 436 | am694methio |
| MAM-2201 | cannabinoid | /sites/default/files/MAM-2201.png | 409 | 528 | mam2201 |
| STS-135 | cannabinoid | /sites/default/files/STS-135v2.png | 391 | 528 | sts135 |
| EAM-2201 | cannabinoid | /sites/default/files/EAM-2201.png | 445 | 528 | eam2201 |
| 5F-PB22 | cannabinoid | /sites/default/files/5F-PB-22.png | 425 | 528 | 5fpb22 |
| AM-694 chloro derivative | cannabinoid | /sites/default/files/AM-694%2520chloro.png | 391 | 436 | am694chlo |
| JWH 018 N-(5-chloropentyl) derivative | cannabinoid | : | : | : | jwh018n5chlo |
| MAM-2201 chloropentyl derivative | cannabinoid | /sites/default/files/MAM-2201%2520N-(5-chloropentyl).png | 409 | 528 | mam2201chlo |
| UR-144 N-(5-chloropentyl) derivative | cannabinoid | /sites/default/files/UR-144%2520N-(5-chloropentyl).png | 391 | 458 | ur144n5chlo |
| JWH 018 N-(5-bromopentyl) derivative | cannabinoid | /sites/default/files/JWH-018%2520N-(5-bromopentyl).png | 391 | 528 | jwh018n5bro |
| AM-2232 | cannabinoid | /sites/default/files/AM-2232.png | 391 | 528 | am2232 |
| A-796,260 | cannabinoid | /sites/default/files/A-796_260.png | 350 | 487 | a796260 |
| JWH-200 | cannabinoid | /sites/default/files/JWH-200.png | 356 | 557 | jwh200 |
| WIN 48,098 / Pravadoline | cannabinoid | /sites/default/files/WIN%252048_098-pravadoline.png | 445 | 466 | win48098pr |
| AB-005 | cannabinoid | /sites/default/files/AB-005.png | 350 | 454 | ab005 |
| AM-1220 | cannabinoid | /sites/default/files/AM-1220.png | 356 | 524 | am1220 |
| AM-1248 | cannabinoid | /sites/default/files/AM-1248.png | 356 | 474 | am1248 |
| AM-2233 | cannabinoid | /sites/default/files/AM-2233.png | 356 | 433 | am2233 |
| JWH-250 1-(2-methylene-N-methyl-piperidyl) derivative | cannabinoid | /sites/default/files/JWH-250%2520Nmpm%2520deriv.png | 409 | 524 | jwh250nmpm |
| CRA-13 | cannabinoid | /sites/default/files/CRA-13.png | 457 | 469 | cra13 |
| JWH-307 | cannabinoid | /sites/default/files/JWH-307.png | 464 | 510 | jwh307 |
| JWH-370 | cannabinoid | /sites/default/files/JWH-370.png | 464 | 510 | jwh370 |
| JWH-368 | cannabinoid | /sites/default/files/JWH-368.png | 493 | 510 | jwh368 |
| JWH-307 bromine analogue | cannabinoid | /sites/default/files/JWH-307%2520bromine.png | 464 | 510 | jwh307bro |
| JWH-030 | cannabinoid | /sites/default/files/JWH-030.png | 310 | 510 | jwh030 |
| JWH-145 | cannabinoid | /sites/default/files/JWH-145.png | 464 | 510 | jwh145 |
| AM-6527 5F derivative | cannabinoid | /sites/default/files/AM-6527%25205F%2520derivative.png | 425 | 528 | am65275fderivative |
| AM-1248 azepane isomer | cannabinoid | /sites/default/files/AM-1248-azepane.png | 358 | 451 | am1248azepaneisomer |
| CUMYL | ring | /sites/default/files/CUMYL%2520R.gif | 207 | 110 | : |
| naphthyl | ring | /sites/default/files/naphthyl%2520core.png | 224 | 144 | : |
| adamantyl | ring | /sites/default/files/adamantyl%2520ring%2520system.png | 157 | 177 | : |
| cyclopropyl | ring | /sites/default/files/cyclopropyl%2520ring%2250system.png | 144 | 177 | : |
| quinolinyl | ring | /sites/default/files/quinolinyl%2520ring%2520system.png | 177 | 225 | : |
| phenyl | ring | /sites/default/files/phenyl%2520ring%2520system.png | 130 | 144 | : |
| 2-methyl (ring-substituent) | ringSubstituent | : | : | : | blank |
| 2-ethyl | ringSubstituent | : | : | : | blank |
| 2-methoxy | ringSubstituent | : | : | : | blank |
| 4-methoxy | ringSubstituent | : | : | : | blank |
| 2-iodo | ringSubstituent | : | : | : | :blank |
| 2-chloro | ringSubstituent | : | : | : | blank |
| 4-methyl | ringSubstituent | : | : | : | blank |
| 4-ethyl | ringSubstituent | : | : | : | blank |
| 4-propyl | ringSubstituent | : | : | : | blank |
| 4-fluoro | ringSubstituent | : | : | : | blank |
| 4-bromo | ringSubstituent | : | : | : | blank |
| 2,2,3,3-tetramethyl | ringSubstituent | : | : | : | blank |
| isopropyl | ringSubstituent | : | : | : | blank |
| tert-butyl | ringSubstituent | : | : | : | blank |
| methyl | tail | /sites/default/files/methylv2.png | 36 | 90 | : |
| propyl | tail | /sites/default/files/propyl.png | 83 | 171 | : |
| butyl | tail | /sites/default/files/butyl.png | 130 | 198 | : |
| pentyl | tail | /sites/default/files/pentyl2.png | 183 | 221 | |
| pent-4-enyl | tail | /sites/default/files/pentenyl%2520tail.png | 130 | 198 | : |
| pentoxy | tail | /sites/default/files/pentoxy%2520tail.png | 177 | 280 | : |
| 4-cyanobutyl | tail | /sites/default/files/4-cyanobutyl%2520T.gif | 156 | 78 | : |
| 5-fluoropentyl | tail | /sites/default/files/fluoropentyl%2520tail.png | 130 | 252 | : |
| 5-chloropentyl | tail | /sites/default/files/chloropentyl%2520tail.png | 130 | 252 | : |
| 5-bromopentyl | tail | /sites/default/files/bromopentyl%2520tail1.png | 130 | 252 | : |
| hexyl | tail | /sites/default/files/hexyl2.png | 177 | 280 | : |
| heptyl | tail | /sites/default/files/heptyl2.png | 177 | 279 | : |
| cyclohexylmethyl | tail | /sites/default/files/cyclohexylmethyl2.png | 177 | 198 | : |
| fluorobenzyl | tail | /sites/default/files/5-FLUOROBENZYL%2520T.gif | 225 | 125 | : |
| methylpiperidin-2-yl methyl | tail | /sites/default/files/methylpiperidin-2-yl%2520methyl%2520tail.png | 195 | 168 | : |
| methylazepan-3-yl | tail | /sites/default/files/methylazepan-3-yl%2520tail.png | 210 | 157 | : |
| tetrahydropyran-4-yl methyl | tail | /sites/default/files/tetrahydropyran-4-yl%2520tail.png | 195 | 139 | : |
| 2-morpholin-4-yl ethyl | tail | /sites/default/files/2-morpholin-4-yl%2520tail.png | 176 | 201 | : |
| indole | core | /sites/default/files/indole.png | 213 | 144 | : |
| indazole | core | /sites/default/files/Indazole%2520core.png | 213 | 144 | : |
| pyrrole | core | /sites/default/files/pyrrole%2520core.png | 124 | 120 | : |
| naphthalene | core | /sites/default/files/naphthylene%2520core.png | 224 | 144 | : |
| 2-methyl (core-substituent) | coreSubstituent | : | : | : | : |
| 5-phenyl | coreSubstituent | : | : | : | : |
| 5-(2-methyl)phenyl | coreSubstituent | : | : | : | : |
| 5-(2-fluoro)phenyl | coreSubstituent | : | : | : | : |
| 5-(2-bromo)phenyl | coreSubstituent | : | : | : | : |
| 5-(3-fluoro)phenyl | coreSubstituent | : | : | : | : |
| methanone | link | /sites/default/files/methanone.png | 117 | 130 | : |
| ethanone | link | /sites/default/files/ethanone.png | 144 | 130 | : |
| carboxamide | link | /sites/default/files/carboxamide%2520linker.png | 144 | 130 | : |
| carboxylate | link | /sites/default/files/carboxylate%2520linker.png | 144 | 130 | : |
| MDMB-CHMICA | cannabinoid | /sites/default/files/MDMB-CHMICA-new.png | 319 | 372 | mdmb-chmica |
| AB-PINACA | cannabinoid | /sites/default/files/AB-PINACAv2.gif | 295 | 414 | ab-pinaca |
| ADB-FUBINACA | cannabinoid | /sites/default/files/ADB-FUBINACAv2.gif | 331 | 387 | adb-fubinaca |
| ADB-PINACA | cannabinoid | /sites/default/files/ADB-PINACAv2.gif | 285 | 431 | adb-pinaca |
| AB-CHMINACA | cannabinoid | /sites/default/files/AB-CHMINACAv2.gif | 295 | 386 | ab-chminaca |
| ADB-CHMINACA | cannabinoid | /sites/default/files/ADB-CHMINACAv2.gif | 290 | 389 | adb-chminaca |
| 5F-MDMB-PINACA | cannabinoid | /sites/default/files/5F-MDMB-PINACA--5F-ADBv2.gif | 312 | 428 | 5f-mdmb-pinaca |
| MDMB-FUBINAC | cannabinoid | /sites/default/files/MDMB-FUBINACAv2.gif | 429 | 394 | mdmb-fubinaca |
| CUMYL-4CN-BINACA | cannabinoid | /sites/default/files/CUMYL-4CN-BINACAv2.gif | 294 | 525 | cumyl-4cn-binaca |
| MO-CHMINACA | cannabinoid | /sites/default/files/MO-CHMINACAv2.gif | 319 | 406 | mo-chminaca |
| carbamoyl | ring | /sites/default/files/Carbamoyl%2520R.gif | 192 | 186 | : |
| methoxycarbonyl | ring | /sites/default/files/methoxycarbonyl%2520R.gif | 255 | 184 | : |
Synthetic cannabinoid Apinaca
A synthetic cannabinoid that belongs to the adamantyl indazolecarboxamide family. It takes its codename from its systematic chemical name: N-(1-adamantyl)-1-pentyl-1H-indazole-3-carboxamide. It was first reported to the EMCDDA in May 2012 in Bulgaria when it was found in a smoking mixture product called ‘White Widow’. This substance also goes by the name ‘AKB-48’, the name of a popular all-girl band from Japan. This substance was critically reviewed by the WHO’s 36th Expert Committee on Drug Dependence in 2014.
Synthetic cannabinoid 5F-APINACA (5F-AKB48)
A synthetic cannabinoid of the adamantyl indazolecarboxamide family. It is chemically related to APINACA. It was first reported to the EMCDDA when it was detected in a herbal smoking mixture seized by Police in Latvia in September 2012. This substance was critically reviewed by the WHO’s 38th Expert Committee on Drug Dependence in 2016. It has been internationally controlled and will be included in Schedule II of the 1971 UN Convention on Psychotropic Substances.
Synthetic cannabinoid AM-2201 indazolecarboxamide analogue
A is a synthetic cannabinoid of the naphthyl indazolecarboxamide family. It was first reported to the EMCDDA in October 2012 by Finland where it was detected as a component in a white powder.
Synthetic cannabinoid Apica
A synthetic cannabinoid of the adamantyl indolecarboxamide family. It takes its codename from its systematic chemical name: N-(1-adamantyl)-1-pentyl-1H-indole-3-carboxamide. It was first reported to the EMCDDA in July 2012 and has been detected in bulk powders and in herbal smoking mixtures.
Synthetic cannabinoid JWH-018
A synthetic cannabinoid of the naphthoylindole family. It was first reported to the EMCDDA in December 2008 by Germany and Austria, being found as an ingredient in different varieties of ‘Spice’ products. JWH-018 is a controlled substance in many EU Member States. This substance is now internationally controlled and listed in Schedule II of the of the 1971 UN Convention on Psychotropic Substances.
Synthetic cannabinoid JWH-018 adamantoyl derivative
A synthetic cannabinoid of the adamantoylindole family. It was first reported to the EMCDDA in February 2011 when it was detected in branded herbal smoking mixtures such as ‘Nuclear Reactor’, ‘Toxic Waste’ and ‘Radio Active’. This substance also goes by the codename AB-001.
Synthetic cannabinoid AM-6527
A synthetic cannabinoid of the naphthyl indolecarboxamide family. It was first reported to the EMCDDA in July 2012 when it was detected by authorities in Finland. This substance has several codenames such as ‘MN24’, ‘NNIE’, ‘NNEI’, ‘NNE1’.
Synthetic cannabinoid PB-22
A synthetic cannabinoid of the quinolinyl indolecarboxylate family. It was first reported to the EMCDDA in November 2012 when it was detected by Finnish customs authorities in a seizure of 54 kilograms of light brown powder. PB-22 also goes by the codename ‘QUPIC’.
Synthetic cannabinoid JWH-022
A synthetic cannabinoid that belongs to the naphthoylindole family. This substance was first reported to the EMCDDA in November 2011 by the United Kingdom. It is normally found along with AM-2201 and it is known to be formed when AM-2201 breaks down metabolically and by thermal decomposition.
Synthetic cannabinoid AM-1220 Azepane Isomer
A synthetic cannabinoid that belongs to the naphthoylindole family. This substance was reported to the EMCDDA in May 2011. It is thought to be a by-product formed during the production of AM-1220.
Synthetic cannabinoid JWH-019
A synthetic cannabinoid receptor agonist that belongs to the naphthoylindole family. It was first reported to the EMCDDA in October 2010 by Finland. It has been found in herbal smoking mixtures and powders on its own and with other synthetic cannabinoids.
Synthetic cannabinoid BB-22
Little is known about this substance, a quinolinyl indolecarboxylate which shares some structural features similar to known synthetic cannabinoids. It was reported to the EMCDDA in January 2013 when it was detected in powders seized by Spanish authorities. BB-22 also goes by the codename ‘QUCHIC’.
Synthetic cannabinoid AM-2201
A synthetic cannabinoid that belongs to the naphthoylindole family. It was first reported to the EMCDDA in January 2011 by Latvian authorities and has been frequently reported ever since. Use of AM-2201 has been associated with convulsions. This substance is now internationally controlled and listed in Schedule II of the of the 1971 UN Convention on Psychotropic Substances.
Synthetic cannabinoid STS-135
A synthetic cannabinoid that belongs to the adamantyl indolecarboxamide family. It was first reported to the EMCDDA in June 2012 by Hungary and has been detected in powders and in branded herbal smoking mixtures such as ‘Armageddon’. STS-135 was the codename for the 135th mission of the American Space Shuttle programme.
Synthetic cannabinoid 5F-PB22
A synthetic cannabinoid of the quinolinyl indolecarboxylate family. This substance was first reported to the EMCDDA in March 2013 by Belgian authorities. Little is known about this novel compound.
Synthetic cannabinoid JWH 018 N-(5-chloropentyl) derivative
A synthetic cannabinoid that belongs to the naphthoylindole family. It was first reported to the EMCDDA by Germany in July 2012 and has been found often in combination with other synthetic cannabinoids in branded herbal smoking mixtures such as ‘Black Jack Silver’, ‘Black Jack Gold’, ‘New Bonzai Sommernight’ and ‘New Bonzai’.
Synthetic cannabinoid JWH 018 N-(5-bromopentyl) derivative
A synthetic cannabinoid that belongs to the naphthoylindole family. This brominated compound was reported to the EMCDDA by Germany in July 2012 when it was identified as one of the synthetic cannabinoids present in a herbal smoking mixture branded ‘XOXO’.
Synthetic cannabinoid AM-2232
A synthetic cannabinoid that belongs to the naphthoylindole family. It is the only synthetic cannabinoid monitored by the EMCDDA where the tail includes a nitrile group. It was first notified to the EMCDDA by Germany in December 2011 when it was identified as a component of a herbal smoking mixture branded ‘Summerlicious’.
Synthetic cannabinoid JWH-200
A synthetic cannabinoid that belongs to the naphthoylindole family. It was first reported to the EMCDDA in December 2009 when it was detected by authorities in Lithuania in a sample seized by border officials. It has since been detected in powders and in herbal smoking mixtures.
Synthetic cannabinoid AM-1220
A synthetic cannabinoid that belongs to the naphthoylindole family. It was first reported to the EMCDDA in May 2011 when it was detected by German authorities in a herbal smoking mixture branded ‘Soulman’.
Synthetic cannabinoid AM-1248
A cannabinoid receptor agonist of the adamantoylindole type. It was first reported to the EMCDDA in September 2012 when it was detected by German authorities in a herbal smoking mixture branded ‘Annihilation’.
Synthetic cannabinoid CRA-13
The first synthetic cannabinoid reported to the EMCDDA that belongs to the naphthoylnaphthalene family. It was reported in January 2011 by German authorities as a minor ingredient in a herbal smoking mixture. CRA-13 also goes by the codenames ‘CB-13’ and ‘SAB-378’.
Synthetic cannabinoid JWH-030
A synthetic cannabinoid of the naphthoylpyrrole family. It was reported to the EMCDDA in March 2013 by German authorities who detected it in a herbal smoking mixture also containing other (related) synthetic cannabinoids such as JWH-307 and JWH-145.
Synthetic cannabinoid A-834,735
A synthetic cannabinoid that belongs to the cyclopropylindole family. It was reported to the EMCDDA in January 2013 by Polish authorities who detected it in herbal smoking mixtures labelled ‘Sunny’ and ‘June Up’.
Synthetic cannabinoid AM-679
A synthetic cannabinoid that belongs to the benzoylindole family. It was reported to the EMCDDA in January 2012 by Italian authorities who detected it in a package of powder that was marked ‘AM XIAO’.
Synthetic cannabinoid JWH-081
A synthetic cannabinoid that belongs to the naphthoylindole family. It emerged in Europe in June 2010 when it was reported to the EMCDDA by Latvia, Germany, Finland, Austria and Norway. It is frequently detected in herbal smoking mixtures, often in combination with other synthetic cannabinoids.
Synthetic cannabinoid JWH-122
A synthetic cannabinoid receptor agonist that belongs to the naphthoylindole family. It was first reported to the EMCDDA in July 2010 by Latvian authorities. It is still present in the market and is often found as a component of herbal smoking mixtures containing multiple synthetic cannabinoids. It has been associated with intoxications in several countries.
Synthetic cannabinoid JWH-182
A synthetic cannabinoid that belongs to the naphthoylindole family. It was reported to the EMCDDA in February 2011 by Danish authorities. This is the only report of this substance in the context of the EU Early warning system.
Synthetic cannabinoid JWH-203
A synthetic cannabinoid that belongs to the phenylacetylindole family. It was first reported to the EMCDDA in October 2010 by Latvian authorities. It has been found in bulk powders and in branded herbal smoking blends such as ‘Aura Chrome’ and ‘Jah RUSH’.
Synthetic cannabinoid JWH-210
A synthetic cannabinoid that belongs to the naphthoylindole family. It was first reported to the EMCDDA in September 2010 by German authorities and has been detected regularly in bulk powders and in herbal smoking mixtures. Interestingly, it has been detected in herbal cannabis samples.
Synthetic cannabinoid JWH-250
A synthetic cannabinoid that belongs to the phenylacetylindole family. It was first reported to the EMCDDA in October 2009 by the German authorties and has remained in the market since then. It has been detected in bulk powders as well as in branded herbal smoking mixtures such as ‘Jamaican Gold’ and ‘Blast off’, frequently in combination with other synthetic cannabinoids. This substance was critically reviewed by the WHO’s 36th Expert Committee on Drug Dependence in 2014.
Synthetic cannabinoid JWH-251
A synthetic cannabinoid from the phenylacetylindole family. It was first reported to the EMCDDA in February 2011 by German authorities when it was the sole cannabimimetic detected in a branded herbal smoking mixture called ‘Aura Silver’.
Synthetic cannabinoid JWH-387
A synthetic cannabinoid belonging to the naphthoylindole family. This brominated compound was reported to the EMCDDA in July 2011 by German authorities who detected it in a white powder. This is the only report of this substance in the context of the Early warning system.
Synthetic cannabinoid JWH-398
A synthetic cannabinoid that belongs to the naphthoylindole family. It was first reported to the EMCDDA by the United Kingdom in October 2009 in 3 separate branded products, each time in combination with other cannabimimetic substances. It is not frequently reported to EMCDDA in the context of the EU Early warning system.
Synthetic cannabinoid JWH-412
A synthetic cannabinoid that belongs to the naphthoylindole family. It was reported to the EMCDDA in August 2011 by the German authorities, however, it has not been reported by any other countries in the context of the EU Early warning system.
Synthetic cannabinoid RCS-4
A synthetic cannabinoid that belongs to the benzoylindole family. The first formal notification to the EMCDDA was in July 2010 by Hungarian authorities, however, prior to this information had been received from Belarus regarding its detection. It is also known by the codenames ‘NRG-4’ and ‘DD001’. Other substances that have been detected with RCS-4 compounds are phenazepam and alphamethyltryptamine. This substance was critically reviewed by the WHO’s 36th Expert Committee on Drug Dependence in 2014.
Synthetic cannabinoid RCS-4 ortho isomer
A synthetic cannabinoid that belongs to the benzoylindole family. As the name suggests, it is closely related to RCS-4. It was first reported to the EMCDDA in April 2011 when it was detected in a sample of powder seized by Swedish authorities. Other substances that have been detected with RCS-4 compounds are phenazepam and alphamethyltryptamine.
Synthetic cannabinoid RCS-4 (C4)
A synthetic cannabinoid that belongs to the benzoylindole family. As the name suggests, it is closely related to RCS-4, differing only by the length of the alkyl ‘tail’. It was reported to the EMCDDA in June 2011 by Hungarian authorities who detected it in a mixture with RCS-4. Other substances that have been detected with RCS-4 compounds are phenazepam and alphamethyltryptamine.
Synthetic cannabinoid UR-144
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family. It was first reported to the EMCDDA in February 2012 by Finland in a bulk powder and Poland in a branded herbal smoking mixture called ‘Magic Tree’. It acts as a selective agonist of the cannabinoid receptor CB2 and is often found in combination with other cannabimimetics. It is also known by the codenames ‘KM X-1’, ‘TMCP-018’, ‘MN-001’, ‘YX-17’. This substance was critically reviewed by the WHO’s 36th Expert Committee on Drug Dependence in 2014.
Synthetic cannabinoid JWH-122 pentenyl 2-methylindole derivative
A synthetic cannabinoid that belongs to the naphthoylindole family. Its first and only report to the EMCDDA was in July 2012 when it was detected in the United Kingdom in a sample that contained other cannabimimetic components. It is thought that this substance may be produced during the synthesis of MAM-2201.
Synthetic cannabinoid JWH-122 pentenyl derivative
A synthetic cannabinoid that belongs to the naphthoylindole family. The first report to the EMCDDA was in July 2012 when it was detected in the United Kingdom in a sample that contained other cannabimimetic components. It is thought that this substance may be produced during the synthesis of MAM-2201.
Synthetic cannabinoid UR-144 (-2H)
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family. It was first reported to the EMCDDA in July 2012 by French authorities in branded herbal smoking mixtures called ‘Fire Ice’, ‘Pulse’, ‘Buzz’ and ‘Tribe’. It is thought that this substance may be produced during the synthesis of 5FUR-144.
Synthetic cannabinoid AB-005
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family. It was first reported to the EMCDDA in November 2012 by German authorities. It was detected in a branded herbal smoking mixture called ‘Star of Fire’. The azepane isomer of AB-005 was also detected in this product.
Synthetic cannabinoid AB-005 azepane isomer
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family. It was first reported to the EMCDDA in November 2012 by German authorities. It was detected in a branded herbal smoking mixture called ‘Star of Fire’ and is thought to be a by-product formed during the production of AB-005 (which was also found in the product).
Synthetic cannabinoid 3-(p-Methoxybenzoyl)-N-methylindole
A synthetic cannabinoid receptor agonist belongs to the benzoylindole family. The one and only report of this substance to the EMCDDA is from Austria in February 2012 when it was detected in a branded herbal smoking mixture called ‘Brooker Limited Edition’. It is thought that this substance is a chemical intermediate formed during the production of RCS-4.
Synthetic cannabinoid UR-144 heptyl derivative
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family. It was first reported to the EMCDDA in April 2013 by Swedish authorities who detected it in a sample of white powder. It is thought that this substance will have similar properties to UR-144, as it differs only by the length of the alkyl ‘tail’.
Synthetic cannabinoid JWH-073
A synthetic cannabinoid belonging to the naphthoylindole family. It was first specifically reported to the EMCDDA by Denmark in March 2009 and has featured prominently in this market since then. It is similar to JWH-018, differing only in the length of the alkyl ‘tail’. It has been found in bulk powders, branded herbal smoking mixtures and also in resinous products. It is a controlled substances in many European countries. This substance was critically reviewed by the WHO’s 36th Expert Committee on Drug Dependence in 2014 and in 2016.
Synthetic cannabinoid JWH-073 methyl derivative
A synthetic cannabinoid belonging to the naphthoylindole family. It was first reported to the EMCDDA in April 2010 by German authorities who identified it in a branded herbal smoking mixture called ‘King B’. It is not frequently found, the only other instance being reported by Italian authorities in a sample that also contained JWH-073.
Synthetic cannabinoid 5FUR-144
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family. It was first reported to the EMCDDA by the Latvian authorities in February 2012. It has been found in the form of bulk powders as well as in herbal smoking mixtures and in resinous products. It is also known by the codename ‘XLR-11’. This substance was critically reviewed by the WHO’s 38th Expert Committee on Drug Dependence in 2016. It has been internationally controlled and will be included in Schedule II of the of the 1971 UN Convention on Psychotropic Substances.
Synthetic cannabinoid AM-694
A synthetic cannabinoid that belongs to the benzoylindole family. It was first reported to the EMCDDA in July 2010 by the Irish authorities, having been detected in a herbal smoking product called ‘Shamrock’.
Synthetic cannabinoid AM-694 ethyl substituted for iodine
A synthetic cannabinoid that belongs to the benzoylindole family. As the name suggests, it is closely related to AM-694. It was reported to the EMCDDA in July 2012 in a sample of herbal smoking mixture from the United Kingdom that contained other derivatives of AM-694 and is thought to be a by-product of attempts at synthetic cannabinoid production.
Synthetic cannabinoid AM-694 methyl substituted for iodine
A synthetic cannabinoid that belongs to the benzoylindole family. As the name suggests, it is closely related to AM-694. It was reported to the EMCDDA in July 2012 in a sample of herbal smoking mixture from the United Kingdom that contained other derivatives of AM-694 and is thought to be a by-product of attempts at synthetic cannabinoid production.
Synthetic cannabinoid MAM-2201
A synthetic cannabinoid that belongs to the naphthoylindole family. It can be viewed as either a ring-methylated derivative of AM-2201 or an alkyl-fluorinated version of JWH-122. It was first reported to the EMCDDA in June 2011 by authorities in the Netherlands, but is currently a common ingredient of herbal smoking mixtures containing other synthetic cannabinoids. It has been reported to be associated with acute transient psychotic episodes.
Synthetic cannabinoid JWH-007
A synthetic cannabinoid that belongs to the naphthoylindole family. It was reported to the EMCDDA by German authorities in May 2011 having been detected in branded herbal smoking mixtures called “Sence” and “Oceanic Herbs”.
Synthetic cannabinoid EAM-2201
A synthetic cannabinoid that belongs to the naphthoylindole family. It can be viewed as either a ring-ethylated derivative of AM-2201 or an alkyl-fluorinated version of JWH-210. It was first reported to the EMCDDA in February 2013 by Swedish authorities in a sample of powder. It has also been detected in herbal smoking mixtures in combination with other synthetic cannabinoids.
Synthetic cannabinoid JWH-015
A synthetic cannabinoid receptor agonist that belongs to the naphthoylindole family. It has been reported to the EMCDDA only once, back in July 2010 when it was detected in a branded herbal smoking mixture called ‘Topaz’ by the authorities in Austria. The herbal material was identified as Damiana (Turnera diffusa).
Synthetic cannabinoid AM-694 chloro derivative
A synthetic cannabinoid that belongs to the benzoylindole family. As the name suggests, it is closely related to AM-694. It was reported to the EMCDDA in December 2011 by German authorities who detected it in a branded herbal smoking mixture called ‘Atomic Bomb’. The product also contained the parent molecule AM-694.
Synthetic cannabinoid MAM-2201 chloropentyl derivative
A synthetic cannabinoid that belongs to the naphthoylindole family. It can be viewed as the alkyl-chlorinated derivative of JWH-122. It was first reported to the EMCDDA in July 2012 in a sample of herbal smoking mixture from the United Kingdom that contained other derivatives of AM-2201 and is thought to be a by-product of attempts at synthetic cannabinoid production.
Synthetic cannabinoid UR-144 N-(5-chloropentyl) derivative
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family, similar in structure to 5FUR-144. It was first reported to the EMCDDA in December 2012 by Hungarian authorities and subsequently in April 2013 by Croatian authorities. In each case, other cannabinoids were present including 5FUR-144./p>
Synthetic cannabinoid A-796,260
A synthetic cannabinoid of the tetramethylcyclopropyl indolyl ketone family. It is structurally related to UR-144 and to 5FUR-144. It has been reported to the EMCDDA on one occasion by Belgian authorities. It acts as a selective potent agonist of the cannabinoid receptor CB2.
Synthetic cannabinoid WIN 48,098/ Pravadoline
A synthetic cannabinoid that belongs to the benzoylindole family. It was detected in May 2011 by both the German and Polish authorities. It has been found in powders and in herbal smoking mixtures, sometimes in combination with other synthetic cannabinoids. It has been shown to be nephrotoxic in an animal model (dogs).
Synthetic cannabinoid JWH-145
A synthetic cannabinoid of the naphthoylpyrrole family. It was reported to the EMCDDA in March 2013 by German authorities who detected it in a herbal smoking mixture also containing other (related) synthetic cannabinoids such as JWH-307 and JWH-030.
Synthetic cannabinoid AM-2233
A synthetic cannabinoid that belongs to the benzoylindole family. It was first reported to the EMCDDA in August 2011 by Finnish authorities after it was detected in a seizure of white powder. It has also been detected in herbal smoking mixtures, on its own and in combination with other synthetic cannabinoids.
Synthetic cannabinoid JWH-250 1-(2-methylene-N-methyl-piperidyl) derivative
A synthetic cannabinoid that belongs to the phenylacetylindole family. It was first reported to the EMCDDA in March 2011 by Polish authorities. It was found in combination with JWH-122 in twenty herbal smoking mixtures such as ‘Red Mercury’, ‘Aztec Thunder’, ‘Zen Ultra’ and ‘Zephyr’.
Synthetic cannabinoid JWH-307
A synthetic cannabinoid that belongs to the naphthoylpyrrole family. It was first reported to the EMCDDA in August 2011 by authorities in Finland. It was detected in a seizure of powder. It has since been detected in several countries in various herbal smoking blends and in combination with other synthetic cannabinoids.
Synthetic cannabinoid JWH-307 bromine derivative
A synthetic cannabinoid that belongs to the naphthoylpyrrole family. It was reported to the EMCDDA in March 2013 by German authorities who detected it in a herbal smoking mixture also containing other (related) synthetic cannabinoids such as JWH-307 and JWH-030.
Synthetic cannabinoid JWH-368
A synthetic cannabinoid that belongs to the naphthoylpyrrole family. It was reported to the EMCDDA by Latvian authorities in February 2013 after it was detected in a bulk quantity of herbal mixture which also contained AM-2201.
Synthetic cannabinoid JWH-370
A synthetic cannabinoid that belongs to the naphthoylpyrrole family. It was first reported to the EMCDDA in February 2012 by Finnish authorities who detected it in a small sample of powder.
AM-6527 5F derivative
A synthetic cannabinoid of the naphthyl indolecarboxamide family. It was first reported to the EMCDDA in November 2013 when it was found in a herbal mixture with AM-6527 and MAM-2201.
AM-1248 azepane isomer
A synthetic cannabinoid belonging to the adamantoylindole family. Reported to hte EMCDDA in September 2013, it is thought to be a by-product formed during the production of AM-1248.
MDMB-CHMICA
An indolecarboxamide that contains a cyclohexylmethyl group. It was first reported to the EMCDDA in September 2014 by the Hungarian focal point when it was detected in a seizure of herbal material. MDMB-CHMICA has been associated with non-fatal intoxications and deaths in Europe. In July 2016, MDMB-CHMICA was risk-assessed by the EMCDDA and subsequently controlled throughout the EU, as of February 2017. The substance has been internationally controlled and will be placed in Schedule II of the of the UN 1971 Convention on Psychotropic Substances.
AB-PINACA
AB-PINACA is an indazolecarboxamide which is structurally related to Apinaca. This compound has also been identified in products sold in Japan. It was first reported to the EMCDDA in May 2013 by Sweden, when it was detected in an herbal mixture seized that also contained 5F-AKB48.
ADB-FUBINACA
ADB-FUBINACA is an indazolecarboxamide. It was first reported to the EMCDDA in November 2013 by the Turkish focal point. It was detected in herbal material seized containing also AB-PINACA and ADBICA. In 2015, tablets containing ADB-FUBINACA were associated with non-fatal intoxications in Hungary.
ADB-PINACA
ADB-PINACA is an an indazolecarboxamide which is structurally related to Apinaca. It was first reported to the EMCDDA in November 2013 by the United Kingdom focal point. ADB-PINACA was associated with an outbreak of non-fatal intoxications in the United States in September 2013.
AB-CHMINACA
AB-CHMINACA is an indazolecarboxamide. It was first reported to the EMCDDA in April 2014 by the Latvian focal point. AB-CHMINACA was detected in a seizure of plastic bags containing herbal material. The EMCDDA is monitoring intensively this substance.
ADB-CHMINACA
ADB-CHMINACA, also known as MAB-CHMINACA, is an indazolecarboxamide. It was first reported to the EMCDDA in September 2014 by the Hungarian focal point when it was detected in a seizure of powder. ADB-CHMINACA was associated with an outbreak of intoxications, including deaths, in the United States in 2015. The EMCDDA is monitoring intensively this substance.
5F-MDMB-PINACA
5F-MDMB-PINACA, also known as 5F-ADB, is an indazolecarboxamide. It was first reported to the EMCDDA in January 2015 by the Hungarian FP when it was detected in a seizure of powder. 5F-MDMB-PINACA has been associated with serious adverse events in Europe. The EMCDDA is monitoring intensively this substance.
MDMB-FUBINACA
MDMB-FUBINACA is an indazolecarboxamide. It was first reported to the EMCDDA in January 2016 by the Hungarian FP when it was detected in a seizure of powder. Products containing MDMB-FUBINACA in the Russian Federation were associated with an outbreak of serious adverse events in 2014.
CUMYL-4CN-BINACA
CUMYL-4CN-BINACA, also known as SGT-78, is an indazolecarboxamide that contains a cumyl group. It was first reported to the EMCDDA in February 2016 by the Hungarian FP when it was detected in a seizure of herbal material. CUMYL-4CN-BINACA has been associated with deaths in Europe. The EMCDDA is monitoring intensively this substance.
MO-CHMINACA
MO-CHMINACA, also known as MO-AMB, is an indazolecarboxamide, which is structurally related to MDMB-CHMICA. It was first reported to the EMCDDA in December 2016 by the Swedish focal point when it was detected in two biological samples.
Sorry…
No additional information on this cannabinoid is currently available. We are in the process of updating our information base and this should be available shortly.
Fakten und Zahlen
- Derzeit werden über 620 neue psychoaktive Substanzen von der EMCDDA mithilfe des EU-Frühwarnsystems überwacht; davon sind 169 synthetische Cannabinoid-Rezeptor-Agonisten.
- Es sind 14 erkennbare chemische Familien synthetischer Cannabinoide bekannt.
- 2008 — JWH-018 war das erste synthetische Cannabinoid, das in einem „Legal High“-Produkt nachgewiesen wurde.
Chemie und Namensgebung synthetischer Cannabinoide
Viele der von der EMCDDA durch das EU-Frühwarnsystem überwachten synthetischen Cannabinoide haben Bezeichnungen, die auf ihre Entdeckung zurückgehen. In einigen Fällen sind diese von den Anfangsbuchstaben der Namen der Wissenschaftler abgeleitet, die die erste Synthetisierung durchgeführt haben: z. B. JWH-Verbindungen nach John W. Huffman oder AM-Verbindungen nach Alexandros Makriyannis. In anderen Fällen erfolgte die Namensgebung nach der Einrichtung oder dem Unternehmen, bei dem die erste Synthetisierung stattfand: So steht das „HU“ der HU-Reihe synthetischer Cannabinoide für Hebräische Universität Jerusalem und „CP“ für Carl Pfizer. Manche Namen wurden wahrscheinlich auch zu Vermarktungszwecken von den Herstellern von „Legal High“-Produkten gewählt. Gute Beispiele dafür sind „AKB-48“ und „2NE1“, alternative Bezeichnungen für APINACA und APICA. „AKB-48“ ist der Name einer bekannten japanischen Girlband, „2NE1“ der einer südkoreanischen. Das synthetische Cannabinoid XLR-11 wurde wohl nach dem ersten Flüssigkeitsraketentriebwerk benannt, das in den Vereinigten Staaten für den Einsatz in Flugzeugen entwickelt wurde, und spielt möglicherweise auf den vom Verkäufer beabsichtigten Effekt beim Konsum der Substanz an.
Mittlerweile erhalten viele Substanzen Kurznamen, die von ihrer chemischen Langbezeichnung abgeleitet sind, beispielsweise APICA von N-(1-Adamantyl)-1-pentyl-1H-indol-3-carboxamid und APINACA von N-(1-Adamantyl)-1-pentyl-1H-indazol-3-carboxamid. Die EMCDDA hat diese Methode systematisiert, um sie auf neu auftretende Substanzen anzuwenden und zu zeigen, wie sich die verschiedenen Bestandteile kombinieren lassen. Die Struktur vieler synthetischer Cannabinoide lässt sich in vier Komponenten untergliedern: Rest, Rumpf, Bindeglied und gebundene Gruppe. Wird jeder Komponente ein Kurzname zugewiesen, kann die chemische Struktur eines Cannabinoids ohne Verwendung der chemischen Langbezeichnung identifiziert werden. Zur Namensgebung für synthetische Cannabinoide, die diesem Muster entsprechen, bietet sich die folgende Syntax an:
GebundeneGruppe — RestRumpfBindeglied
Die Auflistung der Komponenten folgt derselben Reihenfolge wie in den chemischen Langbezeichnungen, z. B. bei APICA: N-(1-Adamantyl)-1-pentyl-1H-indol-3-carboxamid. Ist ein Restsubstituent vorhanden (d. h. 5F), wird dieser am Beginn des Namens angeführt, und die Substituenten der gebundenen Gruppe werden vor der gebundenen Gruppe genannt. Rumpfsubstituenten stehen am Ende des Namens.
Anwendung dieses neuen Systems auf ein vor Kurzem gemeldetes synthetisches Cannabinoid:
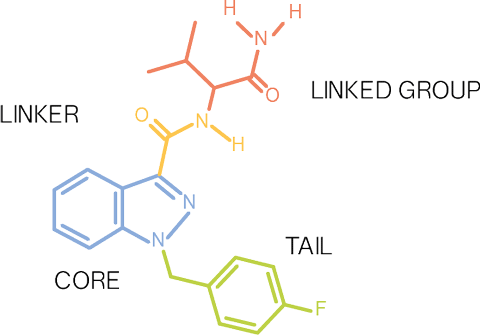
>N-(1-Carbamoyl-2-methyl-propyl)-1-[(4-fluorphenyl)methyl]indazol-3-carboxamid
Aktuelle Bezeichnung: AB-FUBINACA Neue Bezeichnung: MABO-FUBINACA
Für die Buchstabencodes sind nicht nur die verwendeten Buchstaben, sondern auch deren Reihenfolge von Bedeutung. Beispielsweise steht A für das Amin in der gebundenen Gruppe; CA steht für das Carboxamid. Durch Anwendung der beschriebenen Syntax und Kurzformen erhält jedes synthetische Cannabinoid, das diese Struktur aufweist, einen eindeutigen Kurznamen.
- EMCDDA (2015), ‘Synthetic cannabinoids and “Spice” drug profile’, Website der EMCDDA.
- EMCDDA und Europol (2013), EU drug markets: A strategic analysis, gemeinsame Veröffentlichungen der EMCDDA, Amt für Veröffentlichungen der Europäischen Union, Luxemburg.
- Gurney, S. M. R., Scott, K. S., Kacinko, S. L., Presley, B. C. und Logan, B. K. (2014), ‘Pharmacology, toxicology, and adverse effects of synthetic cannabinoid drugs’, Forensic Science Review 26, S. 53–78.
- EMCDDA (2015), ‘New psychoactive substances in Europe. An update from the EU Early Warning System (March 2015)’, EMCDDA, Lissabon, März 2015.
Find out more
Further reading
- EMCDDA (2015), ‘Synthetic cannabinoids and “Spice” drug profile’, Website der EMCDDA.
- EMCDDA und Europol (2013), EU drug markets: A strategic analysis, gemeinsame Veröffentlichungen der EMCDDA, Amt für Veröffentlichungen der Europäischen Union, Luxemburg.
- Gurney, S. M. R., Scott, K. S., Kacinko, S. L., Presley, B. C. und Logan, B. K. (2014), ‘Pharmacology, toxicology, and adverse effects of synthetic cannabinoid drugs’, Forensic Science Review 26, S. 53–78.
- EMCDDA (2015), ‘New psychoactive substances in Europe. An update from the EU Early Warning System (March 2015)’, EMCDDA, Lissabon, März 2015.







